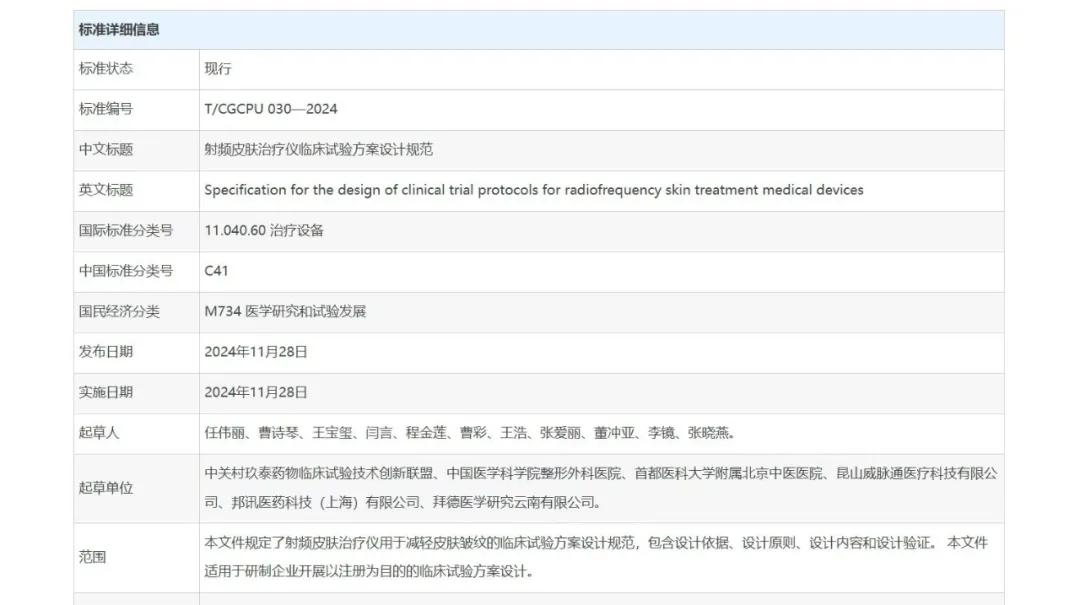
11月28日,《射频皮肤治疗仪临床试验方案设计规范》正式发布实施,标准标号为T/CGCPU 030-2024。该规范由中关村玖泰药物临床试验技术创新联盟提出,联合中国医学科学院整形外科医院、YOUMAGIC研发公司(昆山威脉通医疗科技有限公司)等多家单位共同起草制定。此团体标准的发布标志着我国射频医疗行业向合规化、标准化迈出了重要一步。

国内首个射频临床团体标准发布,为行业创新提供合规化指引
随着人们对抗衰老和变美需求日益增加,射频技术以非入侵、疗效显著、副作用低及广泛的适用性,赢得了广大消费者的青睐,也驱动着诸多企业投身于此类产品的研发与注册。另外随着国家对于医用治疗设备的监管要求日趋完善,行业规范性发展全面提速,进入“械字号”新时期。在此背景下,行业急需一套聚焦射频皮肤治疗仪的临床试验方案设计要求,以规范此类设备的研发与临床应用,推动行业合规和进步。
然而目前,尽管国家药监局器审中心已发布《射频美容设备注册审查指导原则》(2023年第8号),但在具体的临床研究指导原则方面尚属空白。面对合规及标准化需求的紧迫性,YOUMAGIC及研发公司威脉医疗作为行业“先行军”,正发挥自身的技术实力和主观能动性,赋能行业健康发展。
事实上,凭借在射频皮肤治疗领域的深厚积累,YOUMAGIC已率先完成了高能单极射频产品的临床试验,有序开展了动物实验、仿真实验、离体实验及临床试验等相关试验,并成功获批国内首张NMPA三类医疗器械证。

依托在临床试验方面的丰富经验以及多年深耕行业的积累,YOUMAGIC及研发公司威脉医疗为此次团体标准的制定提供了关键的标准依据和理论支持,为行业规范化、和整体研发水平提升给与了关键指引。
构建全面科学可操作的规范框架,推动行业标准化
据悉,《射频皮肤治疗仪临床试验方案设计规范》旨在统一临床试验操作、数据处理、有效性评价、风险防控等关键环节,为射频皮肤治疗仪临床试验构建一个全面、科学且可操作性强的规范框架。
该团体标准基于《药物临床试验质量管理规范》、《医疗器械产品临床试验设计指导原则(2018年第6号)》及《医疗器械临床试验质量管理规范(2022年第28号)》等权威文件,结合射频类皮肤治疗仪的应用原理、产品特性和临床应用需求,制定了详尽的临床试验方案设计规范,适用于研制企业开展以注册为目的的临床试验方案设计。

相关规划遵循“科学性、实用性、独立性、规范性、可操作性”的原则,在设计依据、原则、内容、验证等方面,全方位、多层次地规范了射频皮肤治疗仪的临床试验方案设计流程。为行业内相关临床研究质控提供了统一标准,推动行业的进步、持续创新以及高质量发展。
深化医工结合研发路径,助力产业向健康可持续发展进阶
作为《射频皮肤治疗仪临床试验方案设计规范》的主要起草者之一,该团体标准的发布,也是YOUMAGIC及研发公司威脉医疗重视科研、注重标准的体现。据悉,团队深度参与多种标准的编制工作,并结合自身研发和临床试验经验,提供了坚实的临床技术、临床研究标准和策略指导,助力行业临床研究提质增效。
未来,YOUMAGIC及研发公司威脉医疗将继续深化医工结合研发路径,不断贯彻落实国务院《国家标准化发展纲要》的核心精神,进一步参与和构建行业内临床试验领域的标准化体系,充分激活团体标准在引领临床试验向更高质量跃进中的关键效能,不断为市场发展注入创新活力。
可以预见,随着这一团体标准的深入实施和不断完善,行业将迈入高质量发展阶段,为消费者带来更多前所未有的品质体验,推动产业走向更加合规、健康、可持续的发展道路。
责任编辑:kj005
文章投诉热线:157 3889 8464 投诉邮箱:7983347 16@qq.com