引言:
近年来,免疫治疗成为实体肿瘤治疗的新方法,大量免疫制剂被开发并应用于临床, 其中以免疫检查点抑制剂应用最为广泛,为肿瘤治疗开启了新时代。继程序性死亡受体(PD-1)/程序性死亡配体-1(PD-L1)抑制剂在肿瘤治疗领域的广泛应用后,细胞毒性T淋巴细胞相关蛋白4(CTLA-4)抑制剂进一步丰富了肿瘤免疫治疗方法,开启了肿瘤双免疫疗法的全新治疗模式。
CTLA-4与PD-1双免合璧,实现1+1>2的协同抗肿瘤作用
CTLA-4是影响T细胞功能的关键抑制性受体,与CD28同源,主要表达于活化的CD8+T细胞表面。T细胞表面的CD28分子与抗原呈递细胞(APC)表面的B7-1(CD80)或B7-2(CD86)分子与结合后产生刺激性信号,激活T细胞受体信号通路,使CTLA-4高表达并竞争性结合B7-1/2,从而发挥负性调控作用,抑制T细胞活化。而调节性T(Treg)细胞可通过CTLA-4下调CD80/CD86的表达水平,进而抑制CD28共刺激信号通路,促进肿瘤的发生和发展。CTLA-4抑制剂主要在T细胞反应早期阶段(通常发生在淋巴结中)发挥作用,通过阻断CTLA-4与CD80/CD86的相互作用促进T细胞初始活化,扩大免疫应答广度并增强克隆多样性;而PD-1抑制剂则T细胞反应后期发挥作用,在肿瘤微环境等外周组织中通过抑制PD-1与PD-L1的相互作用维持T细胞功能。这两种药物协同作用可全面调控T细胞活化及效应过程,最终增强T细胞增殖与功能,发挥抗肿瘤作用。此外,CTLA-4抑制剂还具有独有的清除调节性T(Treg)细胞功能,可进一步增强免疫攻击。因此,同时阻断CTLA-4与PD-1,在协同激活抗肿瘤T细胞的同时,还可自身攻击T细胞,起到1+1>2的作用。
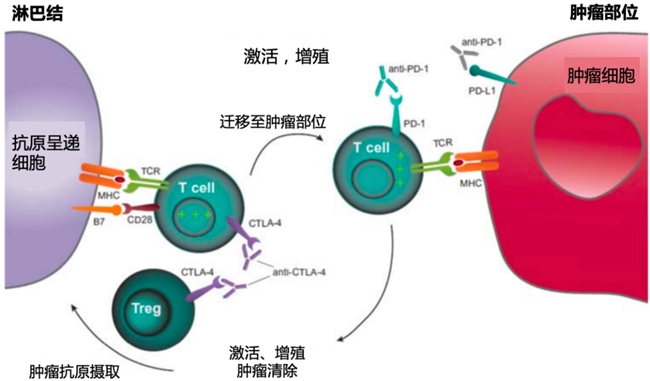
图1. CTLA-4与PD-1通路阻断
广泛获益,CTLA-4联合PD-1抑制剂助力多瘤种生存获益提升
目前在非小细胞癌、结直肠癌、胃/食管癌、肝细胞癌、鼻咽癌、黑色素瘤、肾透明细胞癌等多个实体肿瘤中,多项临床试验已证实CTLA-4抑制剂联合PD-1抑制剂能够在安全可控的基础上,通过互补机制增强T细胞的抗肿瘤能力,为肿瘤患者带来潜在的生存获益。
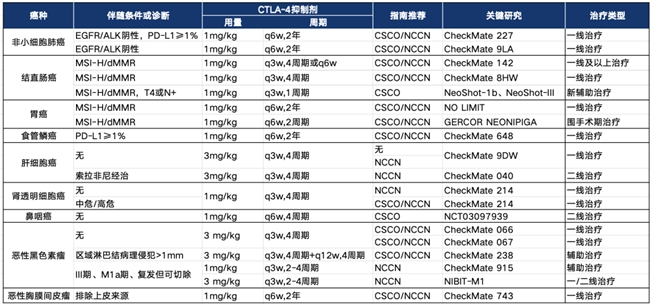
表1. CTLA-4/PD-1双免方案在不同实体肿瘤中的探索
高效低毒,CTLA-4抑制剂联合PD-1抑制剂是目前肠癌免疫治疗的优选
在结直肠癌领域,对于免疫治疗敏感的微卫星高度不稳定性(MSI-H)/错配修复缺陷型(dMMR)患者,KEYNOTE-177研究确立了免疫在一线治疗中的地位,但免疫单药疗效存在一定局限。II期CheckMate 142研究显示,CTLA-4抑制剂联合PD-1抑制剂双免晚期一线治疗可带来持续的肿瘤缓解和长期生存获益:客观缓解率(ORR)突破71%,5年无进展生存(PFS)率达55%,5年总生存(OS)率达67%。在CheckMate 142研究的基础上,III期CheckMate 8HW研究进一步确证了PD-1抑制剂联合伊匹木单抗双免治疗对比PD-1抑制剂单免治疗或化疗的优效性,结果显示,一线双免联合组较单免或化疗组均显示出具有临床意义的PFS改善(双免 vs 化疗PFS 风险比[HR]=0.21,双免 vs 单免PFS HR=0.69),单免组中位PFS已达60.8个月,双免联合组中位PFS尚未达到(NR),但目前已经突破5年有望达到更长的获益;且经过长期随访,双免联合治疗安全性良好,3/4级治疗相关不良事件(TRAEs)发生率为24%,未出现新的安全性信号或额外治疗相关死亡病例。虽然III期COMMIT研究证实免疫治疗联合传统化疗及靶向治疗(阿替利珠单抗+化疗+贝伐珠单抗)一线治疗MSI-H/dMMR转移性结直肠癌,较单免治疗(阿替利珠单抗)亦具有显著PFS获益(HR=0.439),但该PD-L1抑制剂联合化靶方案中位PFS仅24.5个月,远不及双免联合方案以及PD-1抑制剂单药方案的PFS;且PD-L1抑制剂联合化靶方案≥3级AEs发生率高达82.9%,治疗的获益及安全性仍需谨慎评估。
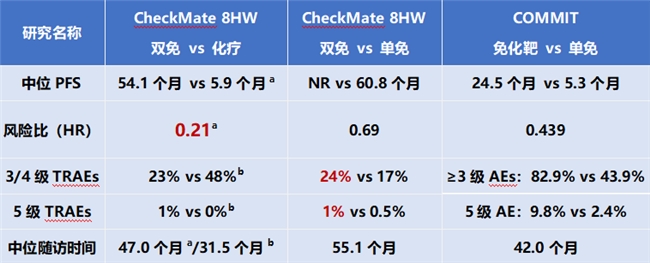
表2. CheckMate 8HW和COMMIT研究PFS和 ≥3级TRAEs或AEs发生率汇总
(HR越低,PFS获益程度越高)(非头对头研究,仅作数据罗列展示)
“好药要先用”:治疗前移,双免治疗有助结直肠癌实现器官保留,带来长生存获益
俗话说:“好药要先用”。目前,双免联合治疗在MSI-H/dMMR结直肠患者的优异疗效已在多项RCT研究中得到反复验证,但在哪一阶段应用才能最大限度提升患者的获益?是临床关注的重点问题。
从双免治疗MSI-H/dMMR晚期结直肠患者的临床研究结果中,我们发现在CheckMate 142研究中,双免一线治疗ORR达71%,疾病控制率(DCR)达84%,5年PFS率为55%;二线及以上治疗ORR为65%,DCR为81%,4年PFS率为53%,显示双免一线使用的疗效优于二线及后线使用。在CheckMate 8HW研究中,尽管一线化疗组有46%的患者后续交叉接受双免治疗,但其中位第二次无进展生存期(PFS2)仍显著劣于双免一线组(中位PFS2:未达到 vs 30.3个月,HR=0.28)。这些结果强调了双免治疗前移的重要性,治疗的早期介入或能有效提升患者的生存获益。
对于可切除的局部晚期MSI-H/dMMR结直肠癌,通常需要进行围手术期的多学科综合治疗。而传统的围手术期化疗疗效十分有限,FOxTROT研究长期随访数据显示,70%的dMMR结肠癌患者对围手术期化疗无应答,病理完全缓解(pCR)率仅为4%,3年复发率仍有20%,患者的治疗需求远未被满足。近年来,多项研究显示,对于MSI-H/dMMR结直肠癌患者,术前予以免疫治疗可观察到较高的pCR率和器官保留潜力。II期NICHE-2研究证实,dMMR结肠癌患者术前接受PD-1抑制剂+伊匹木单抗治疗,pCR率达68%,3年无病生存(DFS)率高达100%,可有效改善患者预后,展示出良好的应用潜力。我国自主研发的伊匹木单抗N01,为国内首个获批联合PD-1单抗用于MSI-H/dMMR结肠癌新辅助治疗的CTLA-4抑制剂,其NeoShot III期注册临床研究显示,伊匹木单抗N01联合信迪利单抗2周期新辅助治疗,pCR率高达82%,显著高于历史对照方案(P<0.0001);相较于手术组,联合方案术后需要辅助治疗的患者比例降低12倍(1.6% vs 21.3%),有助于更多患者免于术后辅助治疗;并且其安全性良好,未明显增加额外安全性风险,无导致手术取消的治疗期间出现的不良事件。该方案为MSI-H/dMMR结肠癌患者提供了一种高效且安全性良好的新辅助治疗选择。
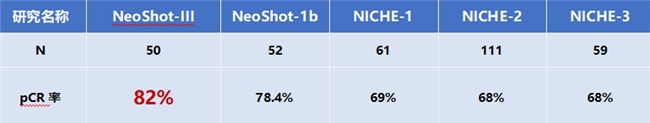
表3. 不同CTLA-4/PD-1双免方案新辅助治疗MSI-H/dMMR结肠癌研究的pCR率汇总(仅作数据罗列,非头对头示意图)
未来,随着双免治疗关口进一步前移以及“观察等待”策略的成熟,我们有理由期待更多结直肠癌患者能在保住器官功能的同时,实现长期生存获益。
免疫为基石,开启结直肠癌治疗新局面
dMMR或MSI-H属于对免疫治疗敏感的“热肿瘤”人群,但是其在结直肠癌中所占的比例仅为10%~15%,占更大比例的错配修复正常(pMMR)或微卫星稳定(MSS)的患者的患者为免疫治疗不敏感的“冷肿瘤”人群,免疫单药疗效一般。目前双免联合治疗在这部分人群中也展开了积极的探索,初步展示出良好的应用前景。
晚期pMMR/MSS患者中的探索
一项II期研究(NCT05608044)显示,新型CTLA-4抑制剂(Botensilimab,BOT)联合PD-1抑制剂(Balstilimab,BAL)二线及以上治疗无肝转移的MSS 转移性结直肠癌患者,总体ORR高于BOT单药组,其中BOT 75 mg/BAL 240 mg组的ORR最高,达19%;安全性良好,≥3级TRAEs的发生率为35%,未观察到新的安全信号,也未发生治疗相关死亡病例。该研究的积极结果支持未来在全球Ⅲ期研究中对该双免方案进一步评估。
早期pMMR/MSS患者中的探索
在pMMR/MSS结肠癌患者中,双免联合治疗的探索也在不断前移。在II期NEST研究显示,BOT联合BAL新辅助治疗pMMR/MSS结肠癌,NEST-1组(联合治疗2周期)pCR为14%,MPR 29%;NEST-2组(联合治疗4周期)pCR为40%,MPR为47%。UNICORN伞式平台研究表明,BOT联合BAL新辅助治疗pMMR/MSS结肠癌pCR达29%,MPR达36%。
2025年发表在Nature杂志的II期NICHE-1研究表明,在31例Ⅰ-Ⅲ期的pMMR结肠癌患者中,PD-1抑制剂联合伊匹木单抗新辅助治疗后手术,8例(26%)的患者观察到治疗缓解,其中6例(20%)患者达到主要病理缓解(MPR)。生物标志物探索分析发现,所有患者的肿瘤突变负荷(TMB)均较低(0.8-8.8 mutations/Mb),但应答者中基因组不稳定评分、染色体基因组不稳定性评分(中位值0.83 vs 0.40)和全基因组复制事件(75% vs 43%)发生率更高。进一步分析发现,TP53突变在应答者中更常见(88%);对比TP53野生型/KRAS G12突变肿瘤(14%)和KRAS G12突变肿瘤(0%),TP53突变/KRAS G12野生型肿瘤可能具有更高的治疗应答富集性(46%),并且TP53突变应答者的细胞增殖标志物评分高于非应答者,提示TP53突变可能为独立的治疗反应预测性生物标志物。此外,应答者体内Ki-67+ CD103+和CD8+ T细胞浸润程度更高,尽管这些细胞在总T细胞池中所占比例相对较小,但保留了增殖能力,被认为参与肿瘤控制,并且与pMMR患者的良好预后和肿瘤反应性相关。
总之,双免治疗的“蓝海尝试”——勇闯结直肠癌“冷肿瘤”冰封之境,为更多结直肠癌患者带来了新的治疗希望。以上研究结果均提示,双免治疗对pMMR/MSS结直肠癌患者有效,有望为这部分患者提供有效去化疗策略。但当前需要更多大样本的随机对照研究验证,以及进一步明确可预测疗效的生物标志物,筛选双免联合治疗优势人群。
权威认证,双免治疗结直肠癌获国内外权威指南一致推荐
目前CTLA-4抑制剂+PD-1抑制剂双免联合用于MSI-H/dMMR结直肠癌,已获得国内外多个权威指南的高度认可。对于晚期MSI-H/dMMR结直肠癌患者的一线、二线及以上治疗,2026年V2版NCCN指南将双免治疗作为2A类推荐方案;对于T4期或肿瘤体积较大的可切除dMMR/MSI-H结直肠癌,新增“考虑新辅助免疫检查点抑制剂治疗”的选项,将术前新辅助治疗进行了完善。同样地,2026年CSCO结直肠癌诊疗指南中:对于MSI-H/dMMR转移性结肠癌,双免联合治疗在潜在可切除者中为I级推荐;在姑息治疗组的一线治疗为I级推荐;姑息治疗组的二/三线治疗,在一线未使用免疫检查点抑制剂者中,双免联合治疗为III级推荐。此外,2026年该指南的重大更新为:对于cT4或N+的可切除MSI-H/dMMR结肠癌患者,先行信迪利单抗联合伊匹木单抗N01治疗,然后进行根治性手术,新增为I级推荐方案。
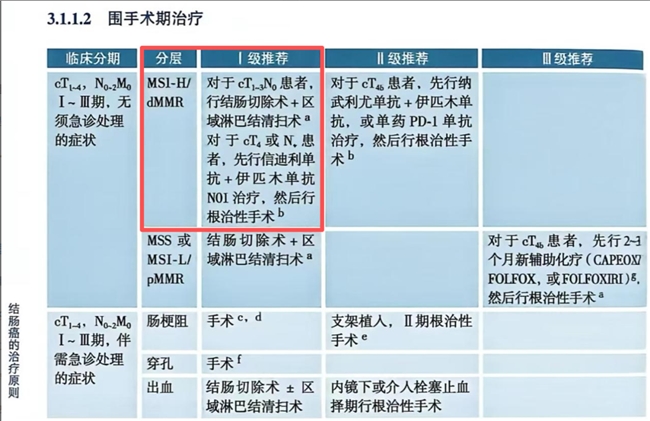
图2. 2026 CSCO结直肠癌诊疗指南非转移性结肠癌围手术期治疗推荐
总结
综合现有循证医学证据与真实世界实践,CTLA-4 抑制剂联合PD-1抑制剂的双免策略在不同实体肿瘤中均显示出良好的治疗潜力,治疗也已逐步从“晚期”前移至“围手术期”。对于局晚不可切结肠癌患者,经双免联合治疗亦可进一步转化为肿瘤可切,以进一步延长患者的生存获益。从NeoShot-III研究中可观察到双免联合治疗的转化治疗潜力:NeoShot-III期研究显示,在入组患者中,有70%是局部较晚期的T4患者,同样也实现了非常好的肿瘤降期,术后病理检查发现,接近80%的患者肿瘤细胞完全消失。
除免疫治疗敏感的“热肿瘤”患者,双免联合治疗在免疫“冷肿瘤”患者中亦展开了诸多积极探索。相信未来随着更多循证医学证据的累积,能够进一步探索双免治疗的生物标志物以预测治疗疗效和风险,筛选出治疗优势人群;明确双免联合治疗的治疗方案和时机。
本文转载自微信公众号《CCMTV肿瘤频道》
仅供医学专业人士阅读
免责声明:市场有风险,选择需谨慎!此文仅供参考,不作买卖依据。
责任编辑:kj005
在众多书籍中,《父亲》这本书宛如一颗璀璨的明珠,散发着独特的魅力,值得每一位读者珍藏本书作者穆春雨,虽文化程度不高,但他怀着对父亲的深厚情感,耗时十几年完成这部...
引言:近年来,免疫治疗成为实体肿瘤治疗的新方法,大量免疫制剂被开发并应用于临床, 其中以免疫检查点抑制剂应用最为广泛,为肿瘤治疗开启了新时代CTLA-4与PD...
2026 年 5 月 8 日,智威智能潮州分公司举行成立仪式,公司总经理吴小强先生亲临现场,宣布潮州分公司开始正式运营广州智威智能科技有限公司 成立于2019年...
“你闭上眼睛,别紧张,放松就好在西安爱尔眼科医院的手术室里,曹丽娜主任的声音平静而温和这一刻,医生与家人的双重身份悄然重叠一个困扰多年的&ldquo...
2026年4月24日,在上海气候周2026暨China ESG Alliance举办的“重构未来绿色生产力”专题论坛上,晨光文具正式发布...